- 3상 임상, 전세계 250명 임상참여 환자군 대대적 모집
혈우병 ‘만능치료제’라 불리던, 앨라일람의 치료제(8인자 9인자) ‘피튜시란(fitusiran)’이 임상 도중, 임상환자 사망으로 모든 시험이 중단되었다가 FDA로부터 임상중단 해제 조치를 받게 됐다.
 |
||
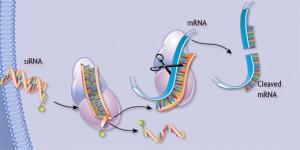
| ▲ Alnylam RNAi | ||
앞서, ‘피튜시란’ 치료제가 혈우병 만능치료제라 일컫는 까닭은 해당물질이 환자 체내에서 응고 과정을 돕는 단백질 ‘트롬빈’의 생산을 증가시켜서 혈액응고를 방해하는 ‘안티 트롬빈’의 농도를 낮추는 방법으로 작용되는 응고과정을 갖고 있기 때문이다. 이에 따라 혈우병 A형 환자와 B형 환자, 나아가 항체 환자들까지 구분 없이 혈액응고를 돕게 되는 새로운 기전의 치료제이다.
혈우병을 치료하는 새로운 접근방법으로 전세계 혈우병 전문가들에게 많은 관심을 받았으나, 지난 9월 경 임상에 참여했던 환자에게서 임상물질과 직접 인과관계가 있는 뇌출혈이 발생해 모든 임상이 중단된 바 있다.
임상이 중단된 후, 연구진들은 임상 프로토콜을 수정해 새로운 투약방법으로 FDA에 개정안을 제출해 지난 주말 승인받았다.
이와관련 앨라일람의 부사장 겸 총책임자 Akin Akinc 박사는 “피튜시란은 혈우병 환자의 삶을 개선 할 수 있는 잠재력을 보유하고 있기 때문에 FDA로부터 임상보류 해제를 받게 됐다”며 “FDA의 결정을 매우 기쁘게 생각한다”고 밝혔다.
FDA의 이번 결정으로 향후 시판을 염두에 둔 3상 임상이 가능하게 된 것이다. 최근까지 진행된 임상은 혈우병 A환자 27명, 혈우병 B환자 6명 등 총 33명의 환자가 참여해 피하주사 방식으로 50mg 또는 80mg의 피튜시란을 투여받았다. 이 연구에서 참가자들은 ‘혈전색전증 없이’ 20개월 동안 ‘고무적인 안전성’을 나타냈다.
◆ 임상환자 대대적 모집
앨라일람은 ‘피튜시란’ 치료제의 임상중단이 해제되면서 임상참여 대상자를 큰 폭으로 모집한다고 밝혔다.
사노피(Sanofi)의 앨라일람의 프로젝트 수석 책임자 Baisong Mei 박사는 “우리는 Alnylam의 동료들과 ‘ATLAS Phase3’ 프로그램을 시작하게 된 것을 기쁘게 생각한다”며 “피튜시란의 안전성과 효능을 평가하기 위해 고안된 ATLAS 연구는 전 세계 100개 이상의 임상센터에서 약 250명의 환자를 등록 할 것으로 예상한다”고 밝혔다.
아울러, 앨라일람의 부사장 겸 총책임자 Akin Akinc 박사는 “추가적인 위험 완화 조치가 시행 되면서 피튜시란의 개발이 더 늦어지지 않기를 기대하며 금년 연말에 투약을 재개할 것으로 기대한다”고 덧붙였다.
[헤모라이프 유성연 기자]
유성연 기자 tjddus@newsfinder.co.kr
